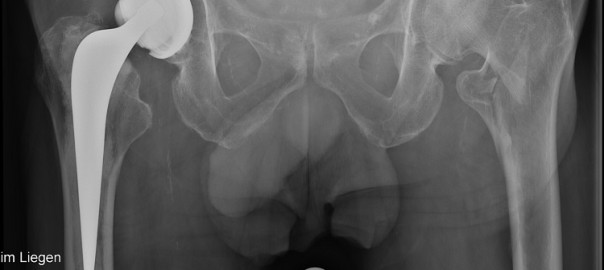
20% der Patienten sterben innerhalb eines Jahres nach einer Hüftfraktur.1 Mit einer frühzeitigen Diagnose und einer gezielten Osteoporose-Therapie lassen sich Frakturen vorbeugen. Die wichtigsten Kriterien zur Risikobewertung, anamnestische Parameter sowie die Wirksamkeit und Verträglichkeit von Prolia® als Therapieoption bei Osteoporose haben wir für Sie zusammengefasst.
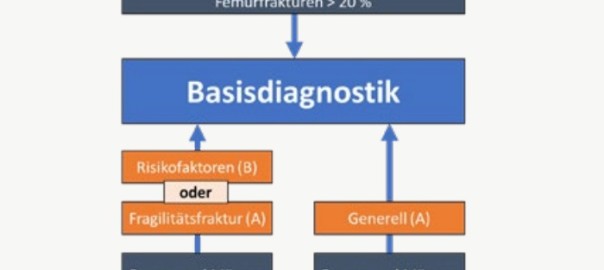
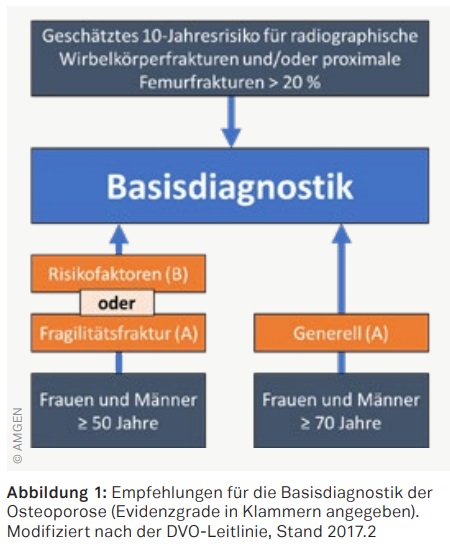
Bei Frauen und Männern ab 50 Jahren, die aufgrund individueller Risikofaktoren ein 10-Jahresrisiko für radiographische Wirbelkörper- oder Hüftfrakturen von >20% besitzen, ist eine Basisdiagnostik zur Abklärung einer Osteoporose indiziert (Abbildung 1).2
Für die Risikobewertung bei postmenopausalen Frauen und bei Männern mit erhöhtem Frakturrisiko hat der DVO ein spezielles Modell entwickelt. Dieses berücksichtigt unter anderem
- das Alter und Geschlecht,
- die Anzahl und den Schweregrad von Wirbelkörperfrakturen in der Vorgeschichte,
- Fragilitätsfrakturen in der Familienanamnese,
- die allgemeine körperliche Verfassung und das Sturzrisiko,
- bestimmte Grunderkrankungen und Medikamente sowie
- krankheitsrelevante Biomarker.2
Anamnese
Die Anamnese kann wichtige Hinweise auf ein erhöhtes Osteoporoserisiko liefern. Wichtige anamnestische Parameter sind:
- Wirbelkörperfrakturen in der Vorgeschichte2
- Akute oder chronische Schmerzsymptomatik2
- Dauer und Zeitpunkt (Tag/Nacht) der Schmerzen
- Komorbiditäten oder Medikation, die eine sekundäre Osteoporose begünstigen2
Knochendichtemessung und Abklärung von Wirbelkörperfrakturen
Eine Knochendichtemessung an der Lendenwirbelsäule und/oder am proximalen Femur ist unerlässlich, um die Verdachtsdiagnose einer Osteoporose zu bestätigen. Als Goldstandard für die Osteodensitometrie hat sich die Dual-X-Ray-Absorptiometrie (DXA) etabliert. Der DXAMesswert wird in Relation zu der Knochendichte von gesunden, jungen Menschen (Alter 20 bis 29 Jahre) desselben Geschlechts gesetzt und als T-Score angegeben. Weicht der T-Score mindestens um -2,5 Standardabweichungen von dem Referenzwert ab, gilt die Diagnose der Osteoporose nach der Definition der Weltgesundheitsorganisation als gesichert.2 Ist eine DXA-Messung nicht möglich oder nur unter erschwerten Bedingungen durchführbar, können auch andere Bildgebungsmodalitäten, wie die Sonographie oder die quantitative Computertomographie (QCT), zum Einsatz kommen.2
Wichtig: Laut DVO-Leitlinie (DVO: Dachverband Osteologie e. V.) sollte bei Männern und Frauen ab dem 70. Lebensjahr grundsätzlich eine Basisdiagnostik zur Abklärung einer Osteoporose erfolgen, sofern „zukünftige, geplante therapeutische Maßnahmen dies rechtfertigen“.2
Klinische Befunde
Die obligatorische körperliche Untersuchung sollte laut DVO-Leitlinie die Gesamtfunktion des Bewegungsapparates, die Muskelkraft, den Body-Mass-Index und die Körpergröße des Patienten beurteilen.2 Auch eine neurologische Untersuchung ist gemäß DVO-Leitlinie sinnvoll, da bei Osteoporose eine spinale Kompressionssymptomatik oder neuromuskuläre Defizite vorliegen können, die mitunter ein erhöhtes Sturzrisiko nach sich ziehen.
Prolia® als mögliche Therapieoption
Eine mögliche medikamentöse Therapieoption der Osteoporose stellt Prolia® dar. Gemäß den DVO-Leitlinien gilt Prolia® mit einer AAA-Bewertung als Firstline-Therapie, die auch in der Langzeitanwendung einen konstanten Zuwachs an Knochenmasse ermöglichen kann und gut verträglich ist.3 Seit dem 26. Mai 2010 ist Prolia® (Denosumab) zur Behandlung der Osteoporose bei postmenopausalen Frauen und bei Männern mit erhöhtem Frakturrisiko in Deutschland zugelassen. Außerdem kann der Wirkstoff hierzulande zur Therapie bei Knochenschwund im Zusammenhang mit einer Hormonablation bei Männern mit Prostatakarzinom mit erhöhtem Frakturrisiko und bei Knochenschwund in Zusammenhang mit einer systemischen Glucocorticoid-Langzeittherapie mit erhöhtem Frakturrisiko eingesetzt werden.4
Prolia® – ein Antikörper in der Osteoporosetherapie
Der vollhumane, monoklonale IgG2-Antikörper Denosumab bindet mit hoher Affinität und Spezifität an den RANKLiganden, der sich auf Osteoklasten befindet. Dadurch wird die Reifung, die Funktion und das Überleben der Osteoklasten gehemmt.4, 7
Auf diese Weise beugt Prolia® sowohl der trabekulären als auch der kortikalen Knochenresorption vor. Prolia® kann das Risiko für Wirbelkörperfrakturen, nicht-vertebrale Frakturen und Hüftfrakturen senken.6 In klinischen Studien wurden keine neutralisierenden Antikörper gegen Prolia® nachgewiesen.4
Wann wird Prolia® eingesetzt?
Die Anwendung von Prolia® erfolgt alle sechs Monate durch eine subkutane Injektion von 60 mg des Wirkstoffs Denosumab in den Bauch, den Oberschenkel oder den Oberarm.4
Eine Dosisanpassung ist weder bei älteren Menschen noch bei Patienten mit einer Nierenfunktionsstörung notwendig. Der Schweregrad einer möglicherweise bestehenden Niereninsuffizienz hat keine Auswirkungen auf die Pharmakokinetik von Denosumab. Bei Patienten mit schwerer Nierenfunktionsstörung (Kreatinin-Clearance <30 ml/min) oder bei dialysepflichtigen Patienten besteht ein höheres Risiko, dass sie eine Hypokalzämie entwickeln.4
Hypokalzämie: vor Therapie den Kalziumwert kontrollieren
Bei der Applikation von Prolia® wurde in zwei placebokontrollierten klinischen Studien der Phase III bei zwei von 4.050 (0,05%) postmenopausalen Frauen mit Osteoporose ein Absinken der Serumkalziumwerte auf weniger als 1,88 mmol/l beobachtet.4 Um dieser seltenen7, aber bedeutenden Nebenwirkung in der Therapie mit Denosumab vorzubeugen, sollte vor Beginn der Behandlung einer Osteoporose mit Prolia® der Kalziumwert bestimmt und bei erniedrigten Serumspiegeln ausreichend Kalzium und Vitamin D substituiert werden.8 Das Risiko für das Auftreten von schweren, symptomatischen Hypokalzämien ist innerhalb der ersten Wochen nach Beginn der Therapie am größten. Daher sollten die Kalziumwerte bei Hochrisikopatienten mit einer Prädisposition für gravierende Hypokalzämien auch in den ersten beiden Wochen nach der Applikation der ersten Dosis Denosumab bestimmt werden.4 Zu den Anzeichen für eine Hypokalzämie zählen zum Beispiel
- eine QT-Zeit-Verlängerung,
- eine Tetanie,
- Krampfanfälle,
- veränderte mentale Zustände,
- Parästhesien,
- Spasmen und Muskelkrämpfe.
Insbesondere Menschen mit einer schweren Nierenfunktionsstörung oder Dialysepflichtigkeit weisen ein erhöhtes Risiko auf, eine gravierende Hypokalzämie zu entwickeln. Bei diesen Patienten ist eine adäquate Kalziumzufuhr entscheidend.4, 8
Fazit: effektive und nebenwirkungsarme Therapie mit Prolia®
Phase-III-Studien zeigten in der Langzeitanwendung von Prolia® anhaltend reduzierte Knochenumbaumarker und geringe Inzidenzen an neuen Wirbelkörperfrakturen
und nichtvertebralen Frakturen. Therapienebenwirkungen und schwere unerwünschte Ereignisse wurden während der gesamten Beobachtungszeiträume selten beobachtet.3, 5, 7
Dokumentation der Therapie mit Prolia®
Es ist zu empfehlen, die medizinischen Entscheidungskriterien (z.B. Anamnese, Kontraindikationen) für die Osteoporose-Therapie mit Prolia® in Form von ICD-10 Codes ausführlich zu dokumentieren. So kann die ärztliche Entscheidung auch zu einem späteren Zeitpunkt nachvollzogen werden. Die verschlüsselte Erfassung von Komorbiditäten der Patientinnen und Patienten kann in diesem Zusammenhang die Dokumentation transparenter gestalten.
Quellen
1. Cooper C. The crippling consequences of fractures and their impact on quality of life.
Am J Med. 1997 Aug 18;103(2A):12S-17S.
2. DVO Leitlinie Osteoporose 2017: Prophylaxe, Diagnostik und Therapie der
Osteoporose bei postmenopausalen Frauen und bei Männern.
URL: https://www.dv-osteologie.org/uploads/Leitlinie%202017/Finale%20
Version%20Leitlinie%20Osteoporose%202017_end.pdf (abgerufen am 28.12.2018).
3. Bone HG, Wagman RB, Brandi ML et al. 10 years of denosumab treatment in
postmenopausal women with osteoporosis: results from the phase 3 randomised
FREEDOM trial and open-label extension. Lancet Diabetes Endocrinol 2017; 5:
513-523. https://www.ncbi.nlm.nih.gov/pubmed/28546097
4. Prolia® Fachinformation. Stand Juli 2019. Verfügbar unter:
https://fachkreise.amgen.de/x_download.php?t=f&n=1&id=116 (abgerufen am
14.08.19).
5. Bone HG, Chapurlat R, Brandi ML et al. The effect of three or six years of denosumab
exposure in women with postmenopausal osteoporosis: results from the FREEDOM
extension. J Clin Endocrinol Metab 2013; 98: 4483-4492.
https://www.ncbi.nlm.nih.gov/pubmed/23979955 (abgerufen am 01.02.2019)
6. Cummings SR, Ferrari S, Eastell R et al. Vertebral Fractures After Discontinuation of
Denosumab: A Post Hoc Analysis of the Randomized Placebo-Controlled FREEDOM
Trial and Its Extension. J Bone Miner Res 2018; 33: 190-198.
https://www.ncbi.nlm.nih.gov/pubmed/29105841 (abgerufen am 01.02.2019)
7. Cummings SR, San Martin J, McClung MR et al. Denosumab for prevention of
fractures in postmenopausal women with osteoporosis. N Engl J Med 2009; 361:
756-765. https://www.ncbi.nlm.nih.gov/pubmed/19671655 (abgerufen am 02.01.19)
8. Amgen GmbH München: Rote-Hand-Brief zu Prolia® 60 mg (Denosumab) vom
03.09.2014; verfügbar unter https://www.akdae.de/Arzneimittelsicherheit/RHB/
Archiv/2014/20140903.pdf (abgerufen am 29.01.2019)