Mit dem zunehmenden Grad der Digitalisierung und der Entwicklung von KI- (Künstlicher Intelligenz) basierten Anwendungen befindet sich die Medizin in einem Wandel. Manuelle Prozesse werden zunehmend durch digitale Prozesse unterstützt. Die Beispiele reichen von der Analyse großer Datensätze über digitale, auf large languagemodels basierenden, Chatbots bis hin zu Vernetzung von internetfähigen Geräten. In Anbetracht dessen ist es naheliegend, dass diese Entwicklungen auch in unserem Fach zu nachhaltigen Veränderungen führen könnte.
Bei genauer Evaluation des ambulanten & klinischen Alltags sind verschiedene Bereiche auszumachen, bei denen die Digitalisierung sowie KI unterstützend wirken kann:
1. Dies sind der große Bereich der KI-gestützten radiologischen Bildauswertung inklusive der Qualitätskontrolle, der Erstellung von Befunden und der selbstständigen Messung von
klinisch relevanten Parametern.
2. Ein weiterer Bereich ist die KI-gestützte operative Planung, welche mittels Navigation und roboterassistierter Chirurgie optimiert werden kann. Dieser Aspekt soll hier mit einem
Fokus auf die spinopelvine Interaktion hauptsächlich behandelt werden.
3. Der dritte Bereich ist die Vernetzung und nachfolgende KIgestützte Analyse von großen Datenmengen, um einer prädiktiven und personalisierten Medizin näherzukommen.
1. KI-gestützte Bildgebung:
Da dieser Bereich im Themenheft an anderer Stelle detailliert analysiert wird, soll hier nur ein grober Überblick gegeben werden: Die diagnostische Radiologie ist einer der ersten Fachbereiche in denen KI-gestützte Anwendungen ihr Potential unter Beweis stellen konnten. KI-Technologien konnten zeigen, dass sie bei der Erkennung und Einstufung von Hüft- und Kniegelenksarthrose, sowie bei der Detektion von Implantatlockerungen im Vergleich zu ausgebildeten Radiologen nicht unterlegen sind.1
Weitere mögliche Entwicklungen in der KI-gestützten Bildauswertung könnten folgende Bereiche darstellen:
- Detektion von Pathologien, um damit die Fraktur– und Tumordiagnostik zu verbessern
- Automatisierte quantitative Analyse der Muskulatur oder der Knochendichte zur Detektion von Sarkopenie und Osteoporose. Hierzu zählen auch Handy-Apps wie der Osteoporoserechner der BVOU mit dessen Hilfe das Osteoporoseassoziierte Frakturrisiko der nächsten 3 Jahre bestimmt werden kann.2
- Einsatz in der Früherkennung und automatisierten Detektion von O&U-spezifischen Pathologien wie bspw. Endoprothesenlockerungen, oder dem Skoliose- oder Arthroseprogress
- KI-Algorithmen können automatisiert mit gleicher Reliabilität und Validität die zeitaufwendige Evaluation der spinalen sagittalen Balance ermöglichen.3, 4
2. KI-gestützte Operative Planung und Ausführung
Digitale Applikationen sind bereits seit längerem Teil unseres Faches: Beispielsweise sind digitale Planungen von Endoprothesen oder achskorrigierende Osteotomien als Standard etabliert. In den letzten Jahren wurde die 2D-Planung weiterentwickelt: Mehrere Unternehmen entwickeln für die präoperative Planung auf CT-basierenden 3D-Anwendungen.5 Ein Unternehmen bietet auf der Basis von stereoradiograpischen Untersuchungen, eine digitale 3D-Planung von Hüftprothesen an. Das Besondere ist, dass hierbei auch funktionelle Interaktionen in der sitzenden und stehenden Position mitberücksichtigt werden, und somit positionsabhängige Veränderungen des spinopelvinen Komplexes Rechnung getragen werden können.6 Die individuelle funktionelle Adaptation kann potenziell die Komplikationsrate in Bezug auf Impingement und Dislokationen reduzieren. Eine weitere Möglichkeit der technischen Unterstützung ist die automatisierte Messung spinaler und spinopelviner Parameter zur präoperativen Planung bei der Korrektur sagittaler Deformitäten. 6 Die Software eines etablierten Medizintechnikherstellers misst die Parameter automatisiert und macht auf der Basis von KI-gestützten Analysen einen Vorschlag für die zu wählenden Osteotomiehöhen und deren Ausmaß. Kombiniert wird dies mit einem Dienstleistungspaket zur digitalen Erfassung des Patientreported Outcome.7
Der nächste Schritt wäre die Kombination von KI-Anwendungen mit der bereits etablierten Navigation und roboterassistierten-Chirurgie. Bislang können intraoperative Navigationssysteme die Chirurgin / den Chirurgen bei der Positionierung von Instrumenten und Implantaten unterstützen und so die Präzision von z. B. Pedikelschrauben in der Wirbelsäulenchirurgie oder den Sägeschnitten in der Knieendoprothetik erhöhen.8 Es gilt an dieser Stelle zu unterscheiden zwischen (häufig CT-gestützter intraoperativer) Navigation und zusätzlicher roboter-assistierter Schraubenplatzierung.9 Ähnliches wie für die Wirbelsäulenchirurgie gilt auch für die Knieendoprothetik. Hier gibt es Systeme, bei denen die Sägeschnitte durch Roboterarme geführt werden und Systeme, die nur eine intraoperative Navigation bieten, um beispielsweise die korrekte Ausrichtung und die optimale Weichteilspannung zu erreichen.
In den bisher gängigen verfügbaren roboter-assistierten Systemen verbleibt die volle Kontrolle weiter bei der Operateurin / dem Operateur. Diese bohren, sägen und setzen die Schrauben unter Zuhilfenahme der Assistenzsysteme. Durch KI-Anwendungen wären intraoperative Vorschläge zur Schraubenplatzierung oder Sägeschnittführung möglich, welche durch den Roboterarm-realisiert werden könnten. Die operative Kontrolle verbliebe aber weiter in der Hand des Chirurgen / der Chirurgin. Vor allem das komplexe Themenfeld der spinopelvinen Mobilität in der Hüftendoprothetik stellt für zukünftige KI-Anwendungen einen Themenbereich dar, in dem durch die Verknüpfung von radiologischen Alignmentdaten, mit den Komplikationsraten und dem Patienten-berichteten Outcome ein Potential für Verbesserungen besteht.
So ist beispielsweise die optimale Pfannenposition bei der Implantation einer Hüftendoprothese bis heute nicht abschließend geklärt. Die definierten Zielbereiche beziehen sich auf eine von Lewinnek et al. im Jahr 1978 veröffentlichte Arbeit.10 Bei der hohen Anzahl an jährlich implantierten Hüftgelenkendoprothesen ist die Senkung der Komplikationsrate und damit auch der Reduktion der Hüftprotheseninstabilität von großer Bedeutung. Möglicherweise können KI-Anwendungen hier einen Beitrag leisten.
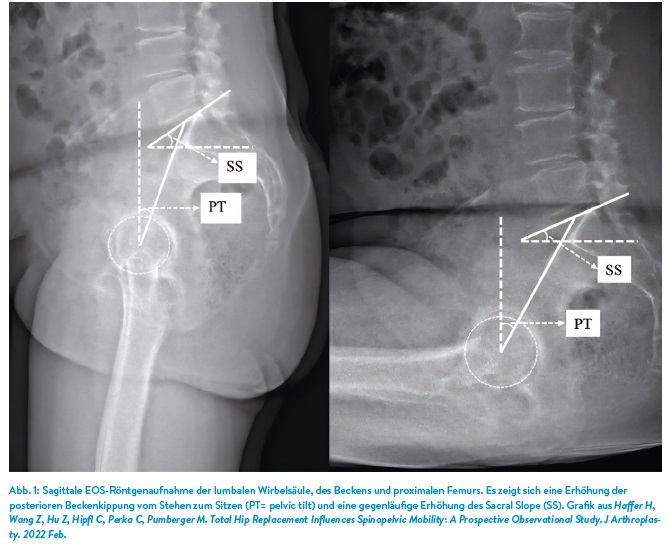
Grundsätzlich kommt es bei Bewegungen zu funktionellen Anpassungen des Achsenskeletts. Beim Hinsetzen kommt es physiologischerweise zu einer posterioren Beckenkippung und damit Erhöhung der azetabulären Anteversion, einer Flexion der Hüftgelenke und einer Reduktion der lumbalen Lordose (Abb. 1). Dies kann als spinopelvine Interaktion beschrieben werden. Aufgrund von Degeneration oder lumbalen Spondylodesen kann es zu einer Veränderung dieses Zusammenspiels kommen, was in eine verminderte Beckenkippung bei Alltagsaktivitäten wie dem Hinsetzen münden kann. Dies birgt im Falle eines Hüftgelenkersatzes das Risiko für ein anteriores Impingement und eine posteriore Dislokation. Übersichtsarbeiten konnten zeigen, dass im Falle einer gleichzeitig bestehenden lumbalen Fusion und eines Hüftgelenkersatzes ein zweifach erhöhtes Risiko für eine Dislokation und ein dreifach erhöhtes Risko für eine Revisionsoperation besteht.11 Aktuell werden verschiedene Risikofaktoren für eine veränderte spinopelvine Interaktion diskutiert. Die Identifikation von Patienten mit einer pelvinen Steifheit ist momentan nur über die radiologische Bestimmung mittels funktioneller Aufnahmen sicher möglich. Ein möglicher KI-Einsatz wäre bei der Identifikation von Risikopatienten, bei denen ein Hüftgelenkersatz geplant ist, denkbar. Diese könnten dann bei Auftreten bestimmter Risikokonstellationen einer radiologischen Diagnostik mittels stehender und sitzender seitlicher Röntgenaufnahmen zur Quantifizierung des pelvinen Steifheit zugeführt werden. KI-Applikationen könnten nachfolgend auch dazu beitragen, eine individuelle Adaptation der azetabulären Komponenten an die spinopelvine Biomechanik in der präoperativen Planung zu ermöglichen.
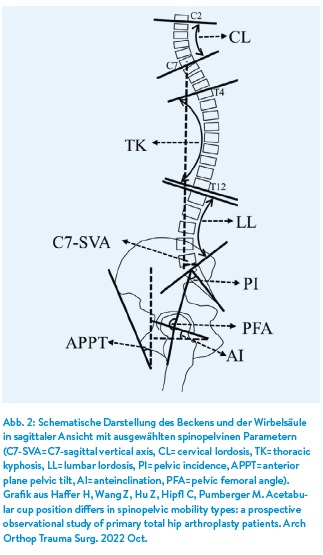
Des Weiteren sollten die spinopelvinen Interaktionen auch im Zusammenhang mit dem sagittalen spinalen Alignment betrachtet werden (Abb. 2). Bis dato sind die komplexen Wechselwirkungen des dreigliedrigen biomechanischen Modells der lumbalen Wirbelsäule, des Beckens und der Hüftgelenke noch nicht abschließend verstanden. Wie oben beschrieben, geht man davon aus, dass eine eingeschränkte pelvine Mobilität die funktionelle Anteversion der azetabulären Komponenten beim Hüftgelenkersatz limitieren kann und hierdurch ein erhöhtes Risiko für ein Impingement und eine Hüftprothesendislokation besteht. Arbeiten der Wirbelsäulenchirurgen Legaye und Duval-Beaupére konnten zeigen, wie bedeutend die pelvine Anatomie für das sagittale Wirbelsäulenprofil ist.12, 13 Vice versa ist jedoch noch nicht abschließend verstanden, inwieweit das sagittale Wirbelsäulenprofil für den spinopelvinen Komplex bedeutsam ist. Beispielsweise kann ein sagittales spinales Malalignment zu einer Reduktion der lumbalen Flexibilität und einer größeren kompensatorischen posterioren Beckenkippung führen, was in der Folge eine anteriore Dislokation der Hüftgelenkendoprothese begünstigen kann.14 Bei Patienten mit adulter spinaler Deformität und bestehendem Hüftgelenksersatz wurde eine Dislokationsrate von 8.0 %, und damit deutlich höher als die in der Literatur üblichen Dislokationsraten beschrieben. Dementsprechend liegt es nahe, dass die funktionelle Implantatausrichtung in der Hüftendoprothetik die gesamte spinopelvine Kette und auch das sagittale spinale Alignment berücksichtigen sollte.
Daher erhofft man sich, dass prädiktive KI-Modelle dazu beitragen, die präoperativen spinopelvinen Wechselwirkungen, als auch postoperative Veränderungen nach chirurgischen Interventionen (Aligmentkorrekturen der Wirbelsäule, Hüftprothesenimplantationen) und deren Einfluss auf die spinopelvine Interaktion besser zu verstehen. Dies könnte auch dazu beitragen, einen Konsens in Bezug auf die optimalen Therapiesequenz bei Hochrisikogruppen mit parallel bestehenden Pathologien der Wirbelsäule und des Hüftgelenkes, wie bei Patienten mit M. Bechterew und Koxarthrose, herzustellen.
Durch die möglicherweise zukünftige KI-gestützte Detektion von Patienten mit Risikokonstellationen, und die intraoperative Adaption an die individuellen anatomisch-biomechanischen Gegebenheiten kann potenziell ein vorzeitiges Versagen der Endoprothese verhindert und ein besseres Patientenoutcome erreicht werden. Diese Anwendungen sind jedoch noch Gegenstand wissenschaftlicher Untersuchungen. Die automatisierte Messung des spinopelvinen Alignments durch KI-Modelle ist jedoch bereits publiziert und scheint mit adäquater Genauigkeit
möglich.15, 16
Ergänzend zu den Einsatzfeldern in der digitalen Planung, intraoperativen Assistenz, und bei der Prädiktion von spinopelvinen Interaktionen, gibt es noch die Möglichkeiten des zukünftigen Einsatzes von virtueller Realität im klinischen Alltag. Das mixed-reality Holografiegerät (HoloLens 2, Microsoft) könnte laut Hersteller zu effizienteren Visiten im Krankenhaus führen.17 Es wäre auch der intraoperative Einsatz, um sich anatomische Landmarken oder die präoperative Bildgebung einblenden zu lassen, denkbar. Dies kann in Kombination mit der navigierten und roboter-assistierten Chirurgie in komplexen
Fällen einen Mehrwert darstellen.
3. Datenvernetzung und KI-gestützte prädiktive Vorhersagen
Die großen Möglichkeiten von KI liegen in der Verarbeitung, Vernetzung und Mustererkennung von Daten. Es wäre denkbar, dass mithilfe von maschinellem Lernen und tiefen neuronalen Netzwerken, die präoperativ (radiologische und klinische Befunde, digitale Gesundheitsanwendungen), intraoperativ (Navigationsdaten, roboter-assistierte Chirurgie) und postoperativ (smarte Implantate, Rehabilitation mit digitalen Gesundheitsanwendungen, digital erfasstes Patient-reported Outome und Registerdaten) gewonnenen Daten miteinander verknüpft werden und so Muster erkannt werden können in Bezug auf bestimmte Risikofaktoren, aber auch positive prädiktive Outcomefaktoren.
Insbesondere die Vernetzung von Digitalen Gesundheitsanwendungen (DiGA) mit der elektronischen Patientenakte (ePA) kann zu einer wertvollen Datenquelle werden. DiGAkönnen über digitale Schnittstellen mit der ePA verbunden werden und Daten einspeisen bzw. erhalten, sodass beispielsweise die Daten aus orthopädischen Wearables, sowie smarten Orthesen und Implantaten hier anschlussfähig sind.18 Digitale Gesundheitsanwendungen (DiGA) können seit Dezember 2019 von Ärztinnen und Psychotherapeuten verordnet und durch die Krankenkassen erstattet werden.19 Aktuell sind in unserem Fach verschiedene DiGAs vom Bundesinstitut für Arzneimittel und Medizinprodukte zugelassen. Diese DiGAs können unterstützend zur konservativen Therapie beispielsweise bei vorderem Knieschmerz, Gonarthrose oder nicht-spezifischen-Rückenschmerzen eingesetzt werden und beinhalten beispielsweise ein individualisiertes Trainingsprogramm, Informationen zur Erkrankung und eine multimodale Therapie. Eine DiGA ist auch zur prä- und postoperativen Anwendung bei Meniskusschädigung und vorderer Kreuzbandruptur zugelassen.20
Weiter kann die KI durch patientenindividuellen Implantatauswahl und Operationstechnik in der Knieendoprothetik oder der gesellschaftlich relevanten Erkrankung des chronischen Rückenschmerzes zur verbesserten Diagnostik und Therapieplanung beitragen.
Bei allen Vorteilen der KI, sind auch die Risiken der neuen Technologie zu beachten. Die KI-Modelle sind in hohem Maße auf eine große, vielschichtige und repräsentative Datenauswahl abhängig. Beinhalten diese einen systematischen Bias, so kann dieser übernommen werden. Beispielsweise eine ausgewogene Berücksichtigung von Faktoren wie dem Geschlecht, der Ethnie und der individuellen Fallschwere müssen hier beachtet werden. Nicht zuletzt sind der Datenschutz und die Datensicherheit von großer Bedeutung. Dem Schutz der Daten muss höchste Priorität eingeräumt werden. Zudem ist eine zunehmende Abhängigkeit der Anwender und Anwenderinnen in O & U von potentiell störanfälliger Technologie zu berücksichtigen.
Zusammenfassend lässt sich feststellen, dass die Medizin im Allgemeinen und die Orthopädie & Unfallchirurgie im Besonderen auf den technischen Fortschritt angewiesen ist. Die Entwicklung von technischer Innovation ist daher grundsätzlich zu begrüßen. Wichtig ist, dass bei der Implementierung von technischer Innovation eine ausgewogene Nutzen-Risikoanalyse vorgenommen wird und der Patientennutzen uneingeschränkt
im Vordergrund steht.

Literatur auf Anfrage bei der Redaktion.