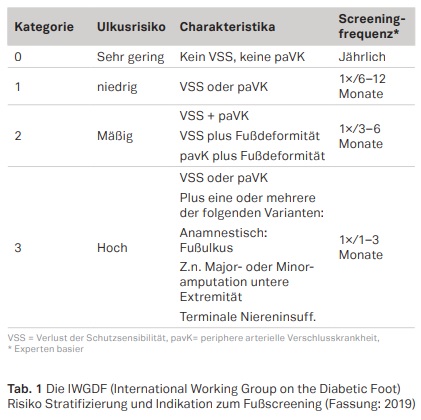
In Kenntnis der Tatsache, dass heute beinahe jeder 10. Deutsche an Diabetes mellitus leidet, sich Zeichen einer diabetischen Neuropathie bei etwa 50% aller Diabetiker nach 25-jähriger Manifestation der Grunderkrankung finden sowie bis zu 25 % aller Diabetiker ein Ulkus im Fußbereich entwickeln können – mit Prävalenz eines diabetischen Fußsyndroms nach fünfjähriger Erkrankungsdauer zwischen 7,6% (Diabetes mellitus Typ I ) und 8,5% (Diabetes mellitus Typ II) – findet sich der Patient auch in der orthopädisch-unfallchirurgischen Praxis. Zudem zählen typische orthopädische Krankheitsbilder wie Hallux valgus, Krallen- und Hammerzehen, Fußdeformitäten in Mittel- und Rückfußbereich, Kontrakturen des M. triceps surae und Einschränkungen der Gelenkmobilität, v.a. im Subtalargelenksbereich, zu den Risikofaktoren in der Ätiopathogenese des diabetischen Fußulkus (Tab. 1). Die lebenslange Inzidenz eines diabetischen Fußulkus liegt zwischen 19 und 34% mit einer jährlichen Inzidenz von 2%. Rezidive nach erfolgreich abgeheilten Ulkus sind mit 40 % pro Jahr zu erwarten, das Risiko steigt auf bis zu 65% binnen einer Frist von drei Jahren. Somit kommt der Prävention des diabetischen Fußulkus überragende Bedeutung zu, wie die wissenschaftlich basierten und 2019 aktualisierten acht Leitlinien der IWGDF (International Working Group on the Diabetic Foot) erkennen lassen.
Zählte früher der Charcotfuß (DNOAP) zu den raren Entitäten, so ist für diese prognostisch ernste Variante des diabetischen Fußsyndroms mit einer Prävalenz über der 1%-Marke zu rechnen. Klinisch bedeutsam wird dies, wenn man berücksichtigt, dass sich hinter mancher scheinbar traumatischen Genese, z. B. unter dem Bild einer OSG-Fraktur, eine DNOAP verbirgt. Zudem sehen wir zunehmend Patienten mit dem klinischen Vollbild eines Charcotfußes, ohne dass überhaupt ein manifester Diabetes mellitus vorliegt bzw. ohne dass wir die Genese der Neuropathie ätiologisch zuordnen können; diese „Charcoide“ machen etwa 10% aus.
Kommt es zum tiefen Infekt,sind Amputationen oft unausweichlich; das diabetische Fußsyndrom bedingt 50–60% aller nicht traumatischen Amputationen an der unteren Extremität, die Inzidenz der Amputationen beim Diabetiker liegt bei 6–8/1000/Jahr, wobei einerseits die Majoramputationen zahlenmäßig abnehmen, die Zahl der Minoramputationen jedoch steigt.
Der richtigen und der rechtzeitigen Diagnosestellung kommt somit wesentliche Bedeutung für den weiteren klinischen Verlauf zu. Eine verzögerte Diagnosestellung ist häufig mit einem deutlich höheren Komplikationsrisiko verknüpft. Darüber hinaus sind klar die Elemente der Prävention des diabetischen Fußsyndroms definiert (Tab. 2).
Diagnostik
Anamnese, Inspektion der Füße, die Inaugenscheinnahme des Schuhwerks, die klinische Prüfung des Gefäßstatus (Gehstrecke, Fußpulse, die Bestimmung des Knöchel-ArmIndex) und die klinische Untersuchung auf das Vorliegen einer diabetischen Neuropathie,sind wegweisend.
Die distale, symmetrische, sensomotorische Neuropathie ist die häufigste Form der diabetischen Neuropathie. Die Diagnostik ist keineswegs nur „ein Fall für den Neurologen“ oder nur mittels neurophysiologischer Diagnostik zu stellen: die Untersuchung mit der Stimmgabel nach Rydel-Seiffer, etwa am Außen- und Innenknöchel zur Beurteilung der Pallästhesie (Vibrationsempfinden), die Prüfung von Spitz-Stumpf-Diskriminierung und Temperatur (kalt-warm)- Empfinden bzw. das Berührempfinden mit dem Semmes-Weinstein-Monofilament 10 g, geben klare Hinweise auf das Vorliegen und den Schweregrad einer Neuropathie.
Selbst wenn es an sämtlichen vorgenannten diagnostischen Hilfsmitteln fehlt, kann die orientierende 1–2 Sekunden dauernde leichte Berührung der Zehen des Patienten und die entsprechende oder fehlende Rückmeldung des Patienten hierzu wesentliche Hinweise für eine Neuropathie ergeben. Dies ist allein schon deshalb bedeutsam, da sie bei über 90% der Ulzerationen am Fuß eine wesentliche Ursache oder Teilursache darstellt und es ohne Neuropathie keine schweren Verlaufsformen wie den Charcotfuß gibt. Ulkogene Risikokonstellationen wie plantare Hyperkeratosen, sind leichter zu therapieren als
das chronische Ulkus. Beim Fußulkus ist der Nachweis einer Verbindung der chronischen Wunde zum Knochen mit dem einfachen „probe to bone“-Test (Kontakt mit einer sterilen Sonde über das Ulkus bis zum Knochen) der Beleg für ein hohes Gefährdungspotenzial,bevor die klassischen klinischen Infektzeichen vorliegen.
Vermeintlich typische klinische Infektzeichen wie die Rötung, Schwellung, Schmerz und Überwärmung können auch Zeichen eines akuten Charcotfußes ohne bakteriellen Infekt sein. Die Differenzierung kann durchfünfminütige Elevation der betroffenen Extremität im Liegen gelingen: beim akuten Charcotfuß geht dann die Rötung und auch ein Teil der Schwellung deutlich zurück, beim Infekt nicht. Bei unauffälligem Röntgenbild in der Frühphase der Erkrankung kann hier die MRT-Bildgebung wegweisend sein, die in fortgeschrittenen Stadien im MRT nicht leicht vom tiefen Infekt zu unterscheiden ist.
Therapie
Neben dem Mantra einer Optimierung des Blutzuckerspiegels und der Co-Morbiditäten, kommt beim diabetischen Fußulkus der Entlastung der betroffenen Extremität – heute typischerweise durch einen nicht abnehmbaren kniehohen Walker mit modularer oder Diabetes adaptierter Einlage – eine wesentliche Bedeutung zu; der klassische „total contact cast“ ist aufwändig und bedarf einer Expertise in der Anwendung, die nicht flächendeckend gewährleistet ist. Abnehmbare und nur knöchelhohe Orthesen sind Patienten mit Kontraindikationen für den hohen und geschlossenen Walker vorbehalten. Voraussetzung für einen Heilerfolg des neuropathischen oder des neuropathisch-ischämischen Ulkus ist eine adäquate regionale Vaskularität, die Entfernung von nekrotischem oder infiziertem Gewebe und die stadiengerechte Infektionskontrolle unter supportiver Antibiotikatherapie oder beim tiefen Infekt mit Progress, Abszess, Gangrän oder gar Sepsiszeichen, auch ein chirurgisches Vorgehen nach den Prinzipien der septischen Chirurgie.
Die Rolle biologisch aktiver Verbandsmittel wird für den Heilverlauf eines plantaren diabetischen Ulkus überschätzt. Chirurgische Konzepte, insbesondere bei Versagen der konservativen Therapieprinzipien, haben ihre Berechtigung und können im Individualfall erhebliche Fortschritte im Heilungsfortgang eines chronischen plantaren Ulkus bedeuten, wenn z. B. die plantare Druckverteilung durch korrigierende Osteotomien, minimalinvasive Achillessehnenverlängerung, Eingriffe zur Verbesserung des Alignements der Zehen (z. B. perkutane Flexortenotomien) oder metatasophalangealen Arthroplastiken verbessert wird. Major-Amputationen sollten, wenn irgendwie möglich, vermieden werden.
Gelenkresektionen oder Metatarsalstrahl(teil-)resektionen können ggf. als „innere Amputation“ unter möglichst weitreichendem Erhalt der wertvollen Fußsohlenhaut erfolgen, wobei der operative Zugang über das Ulkus eine Option eines weichteilschonenden operativen Vorgehens darstellen kann.
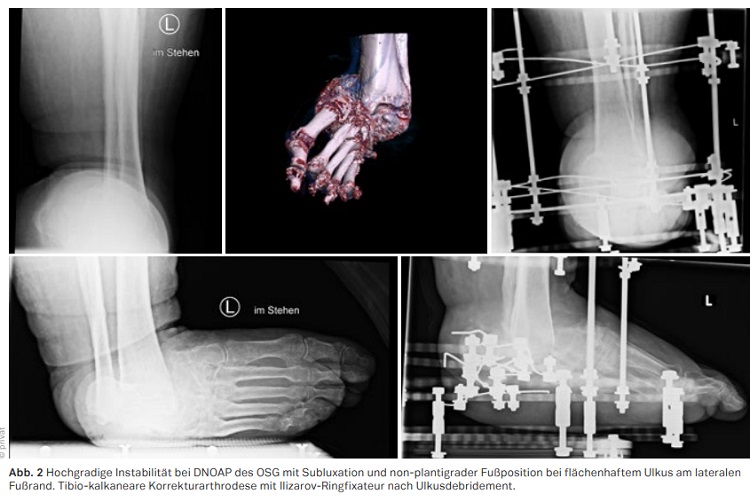
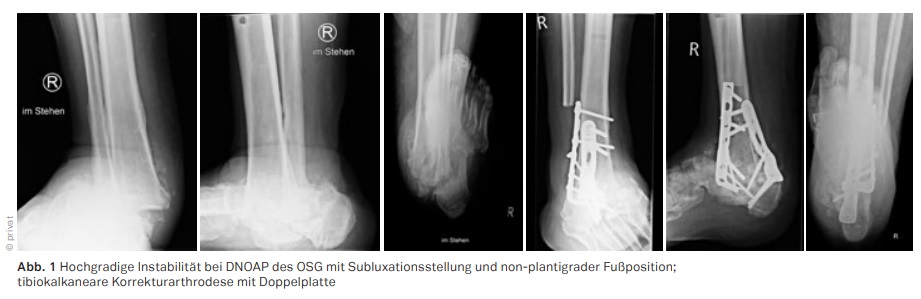
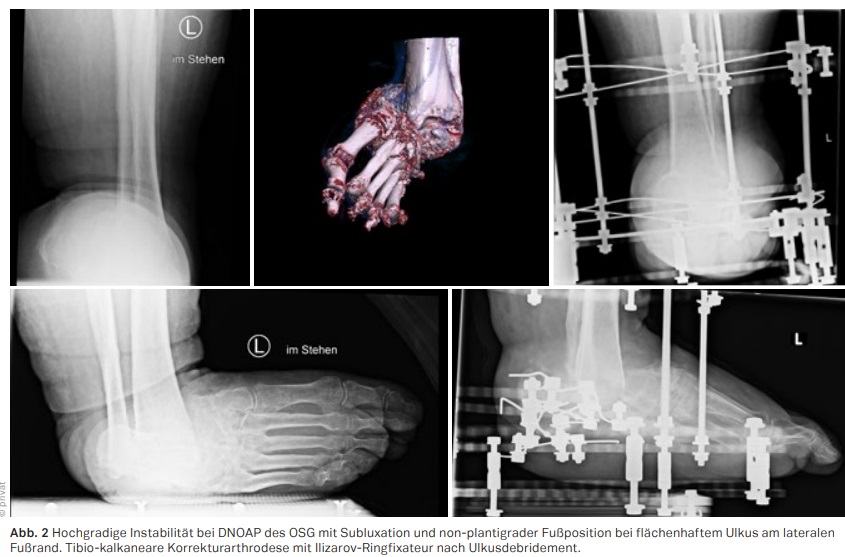
Beim akuten Charcotfuß gilt es die Diagnose so frühzeitig zu stellen, dass durch die ebenfalls frühe Versorgung mit einem kniehohen Walker oder total contact cast die phasenhaft verlaufende Destruktion der Fußtektonik vermieden werden kann. Mit Rückgang der erhöhten lokalen Hauttemperatur und Übergang in ein chronisches Stadium nach Wochen oder Monaten, ist anhand der Kriterien von Instabilität, Fehlstellung und Weichteilkompromittierung zu entscheiden, ob chirurgische Maßnahmen, die von der Exostektomie bis zur Korrekturarthrodese ein weites Feld von Maßnahmen umfassen, die einen langfristigen Extremitätenerhalt unterstützen. Der Befall des Rückfußes ist regelhaft mit einem hohen Grad an Fehlstellung oder Instabilität verbunden und bedarf am häufigsten einer chirurgischen Stabilisation (vgl. Abb. 1 und 2). Die Pathophysiologie der Grunderkrankung macht ein überproportionales Maß an Stabilität erforderlich. Die Heilungszeiten bis zur Konsolidierung sind in der Regel doppelt so lange anzusetzen wie beim Nicht-Diabetiker, wobei auch die Ausbildung einer straffen Pseudarthrose funktionell akzeptable Resultate mit langfristig stabiler plantigrader Fußposition und Extremitätenerhalt gewährleisten kann.
Die regelhafte Kontrolle des Charcotfußes hinsichtlich sich anbahnender Weichteilläsionen oder Überwärmung als Zeichen eines neuen Schubs, ist wesentlicher Teil der Präventionsstrategie, da bei jedem fünften Patienten neue Manifestationen einer DNOAP am ipsi- oder kontralateralen Fuß auftreten.
Dem praktisch tätigen Orthopäden kommt somit durchaus eine relevante Rolle in der Detektion und der Behandlungswahl des diabetischen Fußes, aber eben auch der Prävention, idealerweise in einem interdisziplinären und interprofessionellen Expertenteam zu.
Univ.-Prof. Dr.Thomas Mittlmeier,
Universitätsmedizin Rostock,
Chirurgische Klink und Poliklinik,
Abt. für Unfall-, Hand- und Wiederherstellungschirurgie